Der Artikel beschreibt KI als verbindendes Werkzeug zwischen Forschung und Patientenerfahrung. Er zeigt, wie Systeme des maschinellen Lernens grosse Datenmengen aus Chemie, Biologie, Genomik, klinischen Studien und Versorgung auswerten, um Wirkstoffkandidaten schneller zu finden, Moleküle gezielter zu optimieren, Studien präziser zu planen und bestehende Medikamente für neue Indikationen zu prüfen. Gleichzeitig rücken Patienten stärker in den Mittelpunkt: KI kann passende Studien identifizieren, Therapieentscheidungen unterstützen, Krankheiten früher erkennen, Vitaldaten aus der Ferne überwachen, Therapietreue fördern und Sicherheitssignale nach der Zulassung erfassen. Internationale Beispiele zeigen, dass Fortschritte dort entstehen, wo Pharma, Biotechnologie, Kliniken, Forschung und Technologieanbieter kooperieren. Die Analyse betont Chancen und Verantwortung: KI ist kein Allheilmittel, aber ein Beschleuniger für bessere Evidenz, schnelleren Zugang und personalisierte Versorgung.
Die symbiotischen Auswirkungen von KI auf Arzneimittelentwicklung und Patientenerfahrung in der globalen Pharma- und Biotechnologiebranche
Künstliche Intelligenz (KI) treibt tiefgreifende Veränderungen in der Pharma- und Biotechnologiebranche voran, indem sie gleichzeitig die Arzneimittelentwicklung beschleunigt und die Patientenerfahrung verbessert. Anfang 2020 trat der erste von KI entwickelte Arzneimittelkandidat in klinische Studien am Menschen ein – ein Meilenstein, der die wachsende Rolle der KI in Forschung und Entwicklung signalisierte. Seitdem sind weltweit Dutzende KI-gestützter Programme zur Arzneimittelentdeckung entstanden, wobei bis 2022 mindestens 15 KI-designte Moleküle in der klinischen Entwicklung waren. Parallel dazu ermöglichen KI-gestützte Werkzeuge eine stärker personalisierte Patientenversorgung – von maßgeschneiderten Behandlungen über eine verbesserte Teilnahme an klinischen Studien bis hin zu einem schnelleren Zugang zu neuen Therapien. Dieser Artikel bietet einen analytischen Überblick über zehn zentrale Bereiche, in denen KI sowohl auf die Arzneimittelentwicklung als auch auf die Patientenerfahrung einen symbiotischen Einfluss ausübt, veranschaulicht durch Praxisbeispiele aus Europa, Nordamerika, Japan und Südkorea. Die Erkenntnisse zeigen eine überzeugende und zugleich bescheidene Wahrheit: Wenn KI verantwortungsvoll eingesetzt wird, ermöglicht sie Pharma- und Biotechnologieunternehmen, bessere Medikamente schneller bereitzustellen und gleichzeitig die Versorgung konsequent an den Bedürfnissen der Patienten auszurichten – ein echter Gewinn für Innovation und Gesundheit.
Obwohl meine primäre Fachkompetenz außerhalb der Biotechnologie-, Pharma- und Life-Sciences-Branche liegt, habe ich mich aus einem zutiefst persönlichen und bedeutungsvollen Grund entschieden, diesen Artikel zu schreiben. Vor Kurzem habe ich während eines intensiven Gesprächs mit meiner Frau, Dr. Kolog Gulko – promovierte Wissenschaftlerin des Max-Planck-Instituts – die sich entwickelnden Auswirkungen künstlicher Intelligenz auf die Beschleunigung der Suche nach Lösungen für komplexe Krankheiten erörtert. Unser Gespräch konzentrierte sich insbesondere darauf, wie KI die Arzneimittelentdeckung und -entwicklung transformieren könnte und neue Hoffnung für Erkrankungen bieten kann, für die es heute noch keine endgültigen Heilmethoden gibt.
Dieses Thema berührt mich zutiefst, weil ich seit über 26 Jahren mit Typ-1-Diabetes lebe, die Krankheit zwar erfolgreich behandle, aber stets auf medizinische Fortschritte hoffe. Die Vorstellung, dass KI eines Tages zu schnelleren und präziseren Therapien – oder sogar zu einer Heilung von Typ-1-Diabetes – beitragen könnte, motivierte mich dazu, diesen Beitrag zu recherchieren und zu schreiben. Mein Ziel ist es, eine klare, faktenbasierte Analyse darüber zu liefern, wie KI bereits heute die Arzneimittelentwicklung und die Patientenerfahrung verändert, und zugleich ein umfassenderes menschliches Streben widerzuspiegeln: Heilung zu beschleunigen und das Leben von Menschen durch Innovation zu verbessern.
#1 KI-gestützte Arzneimittelentdeckung: Die Suche nach neuen Therapien beschleunigen
KI hat eine neue Ära der Arzneimittelentdeckung eingeläutet, indem sie neuartige Zielstrukturen und Moleküle mit beispielloser Geschwindigkeit identifiziert. Die traditionelle Arzneimittelentdeckung ist häufig eine langsame und ressourcenintensive Suche nach der Nadel im Heuhaufen. Moderne KI-Systeme hingegen können riesige chemische Bibliotheken und biologische Datensätze durchsuchen, um vielversprechende Wirkstoffkandidaten in einem Bruchteil der Zeit vorherzusagen. Ein wegweisendes Beispiel stammt aus einer japanisch-britischen Zusammenarbeit: Sumitomo Dainippon Pharma und das KI-Biotech-Unternehmen Exscientia gaben im Januar 2020 bekannt, dass ihr gemeinsam entwickelter Wirkstoff DSP-1181 (gegen Zwangsstörungen) als weltweit erstes KI-designtes Medikament in eine klinische Phase-I-Studie eingetreten ist. Bemerkenswerterweise half die KI-Plattform «Centaur Chemist» dabei, DSP-1181 in weniger als 12 Monaten zu entwickeln – eine explorative Forschungsphase, die normalerweise durchschnittlich vier bis fünf Jahre dauert. Diese Leistung, die durch die Kombination der Algorithmen von Exscientia mit der umfassenden Krankheitsexpertise von Sumitomo erzielt wurde, markierte einen entscheidenden Wendepunkt und zeigte, wie KI frühe F&E-Zeitpläne radikal verkürzen kann, ohne die wissenschaftliche Genauigkeit zu beeinträchtigen.
Seit diesem ersten Machbarkeitsnachweis hat die KI-gestützte Arzneimittelentdeckung weltweit rasch an Dynamik gewonnen. Große Pharmaunternehmen gehen zunehmend Partnerschaften mit KI-Start-ups ein, um diese Fähigkeiten zu nutzen. So haben beispielsweise Pfizer und Eli Lilly – zwei der weltweit größten Arzneimittelhersteller – Kooperationen mit dem Silicon-Valley-Unternehmen Atomwise geschlossen, um maschinelles Lernen zur Identifizierung neuartiger kleiner Moleküle gegen schwer zugängliche biologische Zielstrukturen einzusetzen. Ebenso hat das in London ansässige Unternehmen BenevolentAI Partnerschaften mit Novartis (im Bereich Onkologie) und AstraZeneca (im Bereich Nierenerkrankungen) aufgebaut, um KI bei der Entwicklung neuer therapeutischer Strategien einzusetzen. Der Nutzen liegt auf der Hand: KI-Systeme können riesige Datensätze – von Genomprofilen bis hin zu chemischen Strukturen – wesentlich schneller analysieren als Menschen und dabei unerwartete Kombinationen von Wirkstoffen und Zielstrukturen oder Möglichkeiten zur Umwidmung bestehender Medikamente aufzeigen, die Forschende möglicherweise übersehen würden. Durch die Erweiterung des Suchraums und das Lernen aus vergangenen Daten erhöht KI die Trefferquote bei der Wirkstoffentdeckung – also bei der Identifizierung geeigneter Moleküle zur Entwicklung oder Wiederverwendung – und speist dadurch mehr und bessere Kandidaten in die pharmazeutischen Entwicklungspipelines ein.
#2 Intelligentere und schnellere präklinische Entwicklung
Über die Entdeckung neuer Wirkstoffkandidaten hinaus optimiert KI auch die nachfolgenden Phasen der präklinischen Entwicklung, in denen potenzielle Medikamente verfeinert und getestet werden, bevor sie in klinische Studien am Menschen gelangen. In dieser Phase müssen Forschende die Eigenschaften eines Moleküls – etwa Wirksamkeit, Sicherheit und Stabilität – iterativ verbessern, ein Prozess, der traditionell Jahre dauert. KI beschleunigt diesen Zyklus erheblich durch prädiktive Modellierung und generatives Design. So berichtete das südkoreanische Biotech-Start-up Standigm, dass es mithilfe seiner KI-Plattform zur In-silico-Entwicklung und Bewertung von Verbindungen neuartige Leitstrukturen für Arzneimittelprogramme innerhalb von nur sieben Monaten identifizieren konnte. Dieser Ansatz nutzt KI-Algorithmen, um vorherzusagen, wie sich chemische Modifikationen auf die biologische Aktivität auswirken, sodass Laborarbeit nur noch auf die vielversprechendsten Veränderungen konzentriert wird. Ebenso kombinierte Insilico Medicine – ein Biotechnologieunternehmen mit Aktivitäten in Nordamerika und Asien – KI für die Zielstrukturerkennung und das Moleküldesign, um einen neuen antifibrotischen Wirkstoffkandidaten (gegen idiopathische Lungenfibrose) zu entwickeln und ihn in weniger als 30 Monaten bis zur Phase-I-Bereitschaft zu bringen. Im Vergleich zu den fünf bis sechs Jahren, die ein solcher präklinischer Fortschritt häufig benötigt, zeigt der durch KI beschleunigte Zeitrahmen von Insilico eindrucksvoll, wie maschinelles Lernen die Entwicklung verkürzen kann, ohne Qualitätsverluste zu verursachen.
Diese Geschwindigkeitsgewinne gehen nicht zulasten der Innovation – im Gegenteil: KI-Systeme schlagen häufig strukturell neuartige Verbindungen vor, die menschliche Chemiker möglicherweise nicht intuitiv entwickelt hätten. Die ersten drei KI-designten Medikamente, die klinische Studien erreichten (darunter Exscientias DSP-1181 und EXS21546), waren allesamt neuartige Moleküle, die von KI-Plattformen entdeckt wurden. Neuartige chemische Strukturen sind entscheidend für die Bekämpfung von Krankheiten, bei denen bestehende Moleküle versagt haben. Durch die schnelle Generierung und Filterung von Ideen hilft KI Wissenschaftlern dabei, Wirkstoffkandidaten zu entwickeln, die sowohl innovativ als auch erfolgsoptimiert sind – und damit in wenigen Monaten leisten, wofür sonst jahrelange Versuch-und-Irrtum-Experimente erforderlich wären. Dieser intelligentere und schnellere präklinische Entwicklungsprozess bedeutet, dass vielversprechende Therapien früher getestet werden können, was letztlich den Patienten zugutekommt, die auf neue Behandlungsmöglichkeiten warten.
#3 Optimierung des Designs klinischer Studien mit KI
Die Planung einer erfolgreichen klinischen Studie ist ein komplexer Balanceakt: Endpunkte, Patientenkriterien und Protokolle müssen so ausgewählt werden, dass die Wirksamkeit eines Medikaments wissenschaftlich fundiert geprüft wird, während die Studie gleichzeitig praktikabel bleibt. KI erweist sich in dieser Planungsphase als leistungsstarker Verbündeter, indem sie historische Studiendaten und Real-World-Evidence analysiert, um bessere Studiendesigns zu ermöglichen. Modelle des maschinellen Lernens können unterschiedliche Studienparameter simulieren, um Ergebnisse vorherzusagen oder potenzielle Probleme zu identifizieren, noch bevor eine Studie beginnt. Beispielsweise können KI-gestützte Analysen optimale Einschlusskriterien vorschlagen, die die Teilnahmeberechtigung erweitern, ohne die Sicherheit zu beeinträchtigen, oder sie helfen dabei, geeignete Stichprobengrößen festzulegen, indem sie Schwankungen in den Patientenreaktionen prognostizieren. Pharmaunternehmen in Europa und Nordamerika nutzen solche Werkzeuge bereits aktiv; Novartis investierte beispielsweise in das KI-Unternehmen Yseop, um Elemente der Erstellung klinischer Studienprotokolle sowie der Datenstrukturierung zu automatisieren und zu verbessern, mit dem Ziel, den Weg bis zum Studienstart zu beschleunigen. Durch die Nutzung historischer Daten aus zahlreichen früheren Studien kann KI wahrscheinliche Ursachen für Misserfolge erkennen – etwa einen Endpunkt, der nicht ausreichend sensitiv ist, oder eine Patientengruppe, die schlecht auf die Behandlung anspricht – und Forschern ermöglichen, das Studiendesign proaktiv anzupassen.
Eine besonders fortschrittliche Anwendung ist der Einsatz sogenannter «digitaler Zwillinge» oder synthetischer Kontrollarme in klinischen Studien. Anstatt eine große Gruppe von Patienten einem Placebo oder der Standardtherapie zuzuweisen – was kostspielig sein kann und häufig die Rekrutierung von Teilnehmern erschwert –, experimentieren Unternehmen mit KI-Modellen, die als virtuelle Kontrollpatienten dienen. Diese Modelle werden anhand umfangreicher historischer Patientendaten trainiert, um vorherzusagen, wie sich die Kontrollgruppe verhalten würde, wodurch kleinere oder effizientere Studien möglich werden. Regulierungsbehörden beginnen, diesem Ansatz zunehmend offen gegenüberzustehen: In den Jahren 2022 bis 2023 untersuchten mehrere Pilotstudien – darunter Kooperationen von Start-ups wie Unlearn.AI mit europäischen Pharmaunternehmen – den Einsatz KI-generierter Kontrolldaten in Phase-II-Studien zu neurologischen Erkrankungen. Erste Ergebnisse deuten darauf hin, dass solche KI-basierten synthetischen Kontrollarme, sofern sie streng validiert werden, reale Patientenergebnisse sehr genau nachbilden können, wodurch sich die Anzahl der Teilnehmer in Placebogruppen potenziell reduzieren lässt. Dies beschleunigt nicht nur Studien und senkt die Kosten, sondern begegnet auch ethischen Bedenken, da weniger Patienten wirkungslosen Behandlungen ausgesetzt werden. Obwohl sich dieses Feld noch in der Entwicklung befindet, haben KI-optimierte Studiendesigns – von intelligenteren Protokollen bis hin zu virtuellen Patienten – das Potenzial, die Effizienz und Erfolgsquote klinischer Entwicklungen erheblich zu verbessern. Letztlich bedeuten besser konzipierte Studien, dass wirksame Medikamente schneller und mit klarerer Evidenz auf den Markt gelangen und Patienten somit früher zugutekommen.
#4 Verbesserung der Patientenrekrutierung und Studienteilnahme
Die Rekrutierung von Patienten für klinische Studien gilt häufig als einer der größten Engpässe in der Arzneimittelentwicklung. Schätzungsweise 85 % aller Studien haben Schwierigkeiten, rechtzeitig genügend Teilnehmer zu gewinnen, was zu Verzögerungen oder sogar zum Scheitern von Studien führen kann. Genau hier bewirkt KI einen bedeutenden Wandel, indem sie Patienten intelligent mit geeigneten Studien zusammenführt und den Rekrutierungsprozess vereinfacht. Traditionell basiert die Rekrutierung darauf, dass Ärzte die Eignungskriterien von Patienten manuell mit Studienprotokollen vergleichen – ein langsamer und fehleranfälliger Ansatz. KI kann diesen Abgleich automatisieren und skalieren. Ein aktuelles Beispiel aus den Vereinigten Staaten ist TrialGPT, ein großes Sprachmodell, das von Forschern der NIH (National Institutes of Health) entwickelt wurde. TrialGPT wurde darauf ausgelegt, medizinische Unterlagen und Kriterien klinischer Studien zu analysieren, um passende Übereinstimmungen zu finden. In Tests ordnete das System Patienten mit einer Genauigkeit von 87% den geeigneten Studien zu – praktisch auf dem Niveau erfahrener Kliniker (etwa 89-90% Genauigkeit). Noch bemerkenswerter ist, dass dieses KI-System im klinischen Alltag die Sichtung potenzieller Studienteilnehmer um 40% schneller ermöglichte als manuelle Verfahren, ohne dabei an Genauigkeit einzubüßen.
Solche Effizienzgewinne können die Teilnahme von Patienten erheblich verbessern. Patienten erfahren mit höherer Wahrscheinlichkeit von relevanten Studien und nehmen eher daran teil, wenn die Zuordnung schnell und umfassend erfolgt. Darüber hinaus kann KI helfen, Patienten zu identifizieren, die andernfalls möglicherweise übersehen würden. So können Algorithmen des maschinellen Lernens elektronische Gesundheitsakten großer Gesundheitssysteme durchsuchen, um Personen mit bestimmten genetischen Markern oder Krankheitssubtypen zu identifizieren, die den Kriterien spezialisierter Studien entsprechen – und damit einen wesentlich größeren Kreis erfassen, als es einzelnen Ärzten möglich wäre. Dies wurde beispielsweise in onkologischen Studien in Europa gezeigt, bei denen KI-basierte Werkzeuge Pathologie- und Genomikdatenbanken analysierten, um Krebspatienten für innovative Immuntherapie-Studien zu identifizieren und dadurch die Rekrutierungsraten zu erhöhen. Durch die Verringerung des Rekrutierungsaufwands beschleunigt KI nicht nur die Zeitpläne der Arzneimittelentwicklung, sondern verschafft Patienten auch schneller Zugang zu experimentellen Therapien, die lebensrettend sein könnten. In einem sehr konkreten Sinne fungiert KI als Brücke zwischen klinischen Studien und der Patientengemeinschaft und sorgt dafür, dass mehr Menschen die Möglichkeit erhalten, an Forschung teilzunehmen und potenziell von neuartigen Behandlungen zu profitieren.
#5 KI-gestützte Arzneimittelneupositionierung und schnellerer Zugang zu Therapien
Die symbiotischen Auswirkungen von KI auf Arzneimittelentwicklung und Patientenversorgung zeigen sich besonders eindrucksvoll im Bereich der Arzneimittelneupositionierung – also der Suche nach neuen Einsatzmöglichkeiten für bereits bestehende Medikamente. Die Neupositionierung kann die Verfügbarkeit von Therapien für Patienten erheblich beschleunigen, da bekannte Medikamente bereits über etablierte Sicherheitsprofile verfügen. KI hat sich als äußerst effektiv darin erwiesen, Zusammenhänge zwischen Krankheiten und Medikamenten zu erkennen, die menschlichen Forschern möglicherweise verborgen bleiben, und dadurch schnelle Reaktionen auf neue Gesundheitsbedrohungen zu ermöglichen. Ein bekanntes Beispiel ereignete sich während der COVID-19-Pandemie: Anfang Februar 2020 identifizierte ein Team mithilfe der Plattform von BenevolentAI im Vereinigten Königreich das Rheumamedikament Baricitinib als potenzielle Behandlung für schwere COVID-19-Verläufe, indem KI-Modelle dessen entzündungshemmende und antivirale Wirkmechanismen analysierten. Diese Hypothese wurde umgehend veröffentlicht, und bemerkenswerterweise wurde Baricitinib noch im selben Jahr in klinische Studien zu COVID-19 aufgenommen. Bis Ende 2020 und 2021 bestätigten Studien die Wirksamkeit von Baricitinib bei der Verringerung der Sterblichkeit hospitalisierter COVID-19-Patienten, was zu einer Notfallzulassung und dem weltweiten Einsatz als Therapie führte. Was normalerweise Jahre dauern könnte – die Entdeckung und Validierung einer neuen Behandlung – wurde dank der Fähigkeit von KI, Wissen aus wissenschaftlicher Literatur und biologischen Datenbanken in rasanter Geschwindigkeit auszuwerten, auf wenige Monate verkürzt.
Dieser Erfolg verschaffte Patienten nicht nur schneller Zugang zu einer entscheidenden Therapie während einer Pandemie, sondern demonstrierte auch ein grundlegenderes Prinzip: KI kann die Übertragung wissenschaftlicher Erkenntnisse «vom Labor ans Krankenbett» erheblich beschleunigen. Pharmazeutische Forscher integrieren KI-gestützte Neupositionierung inzwischen auch in ihre Strategien für andere Erkrankungen, insbesondere für seltene oder schwer behandelbare Krankheiten. In Japan gibt es beispielsweise Initiativen, bei denen KI eingesetzt wird, um Bibliotheken bereits zugelassener Medikamente gegen neue Zielstrukturen in Bereichen wie neurodegenerativen Erkrankungen zu testen, um herauszufinden, ob bestehende Arzneimittel Patienten mit Alzheimer oder ALS helfen könnten. Ebenso nutzten südkoreanische Forscher Anfang 2020 ein KI-Modell zur Vorhersage antiviraler Kandidaten aus bereits zugelassenen Medikamenten und identifizierten mehrere vielversprechende Moleküle – darunter einige HIV- und Malariamedikamente – gegen das neuartige Coronavirus, was die Priorisierung von Labor- und klinischen Tests in Asien unterstützte. Durch die systematische Bewertung bekannter Wirkstoffe anhand neuer biologischer Erkenntnisse können KI-gestützte Neupositionierungsansätze die jahrelangen Entdeckungs- und präklinischen Testphasen überspringen, die für völlig neue Medikamente erforderlich wären. Für Patienten bedeutet dies potenziell einen deutlich schnelleren Zugang zu wirksamen Therapien – wie im Fall von Baricitinib bei COVID-19 – und verdeutlicht, wie sich die Beiträge der KI zur Arzneimittelentwicklung unmittelbar und in kurzer Zeit in verbesserten Behandlungsergebnissen niederschlagen können.
#6 Präzisionsmedizin: KI passt Therapien individuell an
Eine der wirkungsvollsten Arten, wie KI die Arzneimittelentwicklung mit der Patientenerfahrung verbindet, besteht in der Ermöglichung echter personalisierter Medizin. Jeder Patient ist einzigartig, und Faktoren wie Genetik, Umwelt und Lebensstil beeinflussen, wie Menschen auf Behandlungen reagieren. KI-Algorithmen sind besonders gut darin, Muster in komplexen, mehrdimensionalen Daten zu erkennen – und eignen sich daher ideal, um festzustellen, welche Patienten am meisten von einer bestimmten Therapie profitieren oder welche Behandlungsstrategie für eine einzelne Person optimal sein könnte. In der Onkologie beispielsweise nutzen Forscher KI, um Genomdaten, medizinische Bildgebung und klinische Aufzeichnungen zusammenzuführen und Therapieansprechen vorherzusagen. Eine aktuelle Studie des US-amerikanischen National Cancer Institute und des Memorial Sloan Kettering Cancer Center entwickelte ein KI-Werkzeug, das routinemäßige klinische Daten – etwa Bluttests und pathologische Befunde – analysiert, um Krebspatienten zu identifizieren, die wahrscheinlich auf Immuncheckpoint-Inhibitoren ansprechen. Dieses KI-Modell mit dem Namen SCORPIO kann Patienten kennzeichnen, die von einer Immuntherapie profitieren würden, und solche identifizieren, bei denen dies wahrscheinlich nicht der Fall ist. Dadurch können Ärzte Behandlungspläne personalisieren – etwa indem sie Patienten die Nebenwirkungen einer Immuntherapie ersparen, die ihnen voraussichtlich nicht helfen würde, und stattdessen alternative Ansätze wählen. Erste Ergebnisse zeigten, dass die Vorhersagen der KI bestimmte Standard-Biomarkertests übertreffen konnten, was verdeutlicht, wie maschinelles Lernen eine differenziertere Grundlage für Therapieentscheidungen bietet.
Auch Pharma- und Biotechnologieunternehmen integrieren solche KI-gestützten Stratifizierungsansätze in ihre Arzneimittelentwicklung. Wenn bekannt ist, welche Untergruppen von Patienten am besten auf eine Therapie ansprechen, können Unternehmen gezieltere klinische Studien konzipieren und spezifische Zulassungen anstreben, wodurch Therapien schneller den richtigen Patienten zur Verfügung gestellt werden. Europäische Initiativen wie das Mailänder Krebsinstitut in Italien arbeiten mit KI-Start-ups zusammen, um Algorithmen zu entwickeln, die Patienten auf Grundlage des molekularen Profils ihres Tumors mit dem wirksamsten Krebsmedikament abgleichen – häufig unter Nutzung der Erfahrungen aus Tausenden früherer Fälle in den Trainingsdaten der Modelle. In Japan, wo personalisierte Medizin eine nationale Priorität darstellt, wird KI eingesetzt, um genetische Daten großer Patientenkohorten – etwa aus Biobanken – zu analysieren und Prädiktoren für Arzneimittelwirksamkeit und Nebenwirkungen in bestimmten Patientengruppen zu identifizieren. Dies trägt zur Entwicklung stärker individualisierter Verschreibungsrichtlinien bei. Selbst bei weit verbreiteten Erkrankungen wie Diabetes oder Bluthochdruck kann KI helfen, Therapien anzupassen, indem sie die wahrscheinliche Reaktion eines einzelnen Patienten auf verschiedene Medikamente vorhersagt – auf Basis von Mustern, die aus elektronischen Gesundheitsakten gelernt wurden. Die Symbiose ist hier offensichtlich: Arzneimittelentwickler erzielen bessere Studienergebnisse, indem sie sich auf die Patienten konzentrieren, die am meisten profitieren, und Patienten erhalten Therapien, die auf ihre persönliche Biologie abgestimmt sind, wodurch Erfolgsraten steigen und das Prinzip von Versuch und Irrtum in der Behandlung reduziert wird. KI wirkt somit als Katalysator für das lang angestrebte Ziel der Präzisionsmedizin und bringt pharmazeutische Innovation mit den individuellen Bedürfnissen der Patienten in Einklang.
#7 KI in der Diagnostik: Früherkennung für frühzeitige Intervention
Obwohl Diagnostik auf den ersten Blick nur indirekt mit der Arzneimittelentwicklung verbunden scheint, spielt sie eine entscheidende Rolle für die Patientenerfahrung und die Gesamtwirksamkeit von Therapien – schließlich kann ein Medikament nur helfen, wenn eine Krankheit korrekt und rechtzeitig erkannt wird. KI-Technologien, insbesondere in der medizinischen Bildgebung und Genomik, verbessern Geschwindigkeit und Genauigkeit von Diagnosen erheblich und ermöglichen Patienten dadurch einen schnelleren Zugang zu den richtigen Behandlungen. In Europa werden beispielsweise KI-Systeme eingesetzt, um radiologische Aufnahmen und pathologische Präparate mit bemerkenswerter Genauigkeit zu analysieren. Der britische National Health Service testete die ophthalmologische KI von DeepMind am Moorfields Eye Hospital, die Anzeichen von Augenerkrankungen wie Makuladegeneration oder diabetischer Retinopathie auf Scans ebenso präzise erkennen kann wie erfahrene Ärzte – und entscheidenderweise deutlich früher im Krankheitsverlauf. Eine frühzeitige Diagnose bedeutet, dass diese Patienten Monate oder sogar Jahre früher sehkrafterhaltende Behandlungen erhalten können, was die Behandlungsergebnisse erheblich verbessert. Ebenso haben Krankenhäuser in Südkorea KI-Software wie Lunit INSIGHT in Programme zur Auswertung von Thoraxröntgenbildern integriert, um frühe Anzeichen von Lungenkrebs oder Tuberkuloseknoten zu erkennen. Dies führte zu mehr frühzeitigen Interventionen, bei denen Patienten mit der Therapie beginnen können, solange sich die Erkrankung noch in einem besser behandelbaren Stadium befindet.
Aus Sicht der Arzneimittelentwicklung sind solche Fortschritte in der KI-gestützten Diagnostik symbiotisch, weil sie den Kreis der Patienten erweitern, die von Therapien profitieren können, und gleichzeitig ideale Kandidaten für neue Behandlungen identifizieren. Pharmaunternehmen, die zielgerichtete Krebsmedikamente entwickeln, sind beispielsweise auf die präzise Identifikation von Patienten angewiesen, deren Tumoren die spezifischen molekularen Marker aufweisen, für die das Medikament entwickelt wurde. KI-Algorithmen, die genetische Testergebnisse oder Biopsiebilder analysieren, können diese Marker schneller und umfassender erkennen als manuelle Verfahren. Ein besonders bemerkenswertes Beispiel findet sich bei seltenen Erkrankungen: Diese bleiben oft jahrelang unerkannt, doch KI wird inzwischen eingesetzt, um Muster in Patientendaten zu erkennen, die auf eine seltene Krankheit hindeuten könnten – etwa subtile Auffälligkeiten in Laborwerten oder sogar charakteristische Gesichtszüge, die anhand von Fotografien analysiert werden. Unternehmen wie Sanofi und Takeda haben in KI-Werkzeuge investiert, um «Nadel-im-Heuhaufen»-Patienten mit seltenen genetischen Erkrankungen zu identifizieren, die von neuartigen Therapien oder klinischen Studien profitieren könnten, und sie so mit Behandlungsmöglichkeiten zu verbinden, von denen sie möglicherweise nichts wussten. In Japan nutzte eine Partnerschaft zwischen Krankenhäusern und Technologieunternehmen KI zur Analyse von Millionen Gesundheitscheck-Datensätzen und konnte dadurch erfolgreich Personen mit Bauchspeicheldrüsenkrebs im Frühstadium identifizieren – einer notoriously schwer zu diagnostizierenden Erkrankung. Dadurch konnten diese Patienten chirurgische und medikamentöse Behandlungen erhalten, solange eine Heilung noch möglich war. Durch die Verbesserung diagnostischer Verfahren stellt KI sicher, dass Patienten früher den richtigen Behandlungspfad einschlagen, was wiederum die Erfolgsraten der Therapien erhöht. Daraus entsteht ein positiver Kreislauf: Wirksame Medikamente bestätigen den Nutzen diagnostischer Werkzeuge, und bessere Diagnostik vergrößert die Wirkung der Medikamente.
#8 Patientenüberwachung und Therapietreue durch KI
Sobald Patienten eine Behandlung erhalten – sei es im Rahmen einer klinischen Studie oder der regulären Versorgung –, sind eine kontinuierliche Überwachung und die Förderung der Therapietreue entscheidend für gute Behandlungsergebnisse. KI wird zunehmend eingesetzt, um Gesundheitsdaten von Patienten fortlaufend zu überwachen und rechtzeitige Interventionen zu ermöglichen, wodurch sowohl die Patientenerfahrung als auch die Wirksamkeit von Therapien verbessert werden. Die zunehmende Verbreitung tragbarer Sensoren (wie Smartwatches, Glukosemessgeräte usw.) und häuslicher Gesundheitsgeräte bedeutet, dass ein einzelner Patient täglich Tausende von Datenpunkten erzeugen kann. KI-Algorithmen können diese Datenströme in Echtzeit analysieren, um besorgniserregende Entwicklungen zu erkennen – beispielsweise könnte eine KI feststellen, dass sich Ruhepuls und Gewicht eines Herzinsuffizienzpatienten in einem Muster erhöhen, das typischerweise einem Krankenhausaufenthalt vorausgeht. Ärzte können daraufhin die Medikation anpassen, bevor eine Krise eintritt. Solche prädiktiven Überwachungssysteme, die häufig auf maschinellen Lernmodellen basieren, die mit umfangreichen Datensätzen zu Krankheitsverläufen trainiert wurden, werden derzeit in Nordamerika und Europa erprobt. In einem von der FDA zugelassenen System für Herzinsuffizienzpatienten analysiert eine KI-Plattform des Bostoner Start-ups Biofourmis Daten tragbarer Sensoren und konnte Krankenhauswiedereinweisungen bis zu eine Woche im Voraus vorhersagen. Dadurch werden proaktive Therapieanpassungen möglich, die Patienten stabil zu Hause halten können.
Pharmaunternehmen integrieren diese Werkzeuge zunehmend als Ergänzung zu ihren Medikamenten – ein Trend, der häufig als «Beyond-the-Pill»-Lösungen bezeichnet wird. Besonders im Diabetesmanagement zeigt sich die Verbindung von KI und Arzneimittelverabreichung deutlich: Closed-Loop-Insulinpumpensysteme, die die Insulindosierung automatisch anhand kontinuierlicher Glukosemessungen anpassen, nutzen KI-gesteuerte Regelungsalgorithmen, um bestimmte Funktionen einer gesunden Bauchspeicheldrüse nachzuahmen. Patienten, die solche KI-gestützten Pumpen verwenden, berichten von einer besseren Blutzuckerkontrolle und einer geringeren Belastung durch das Krankheitsmanagement, was ihre Therapieerfahrung erheblich verbessert. Ein weiterer wichtiger Bereich ist die Therapietreue – also die korrekte Einnahme von Medikamenten –, bei der KI sowohl Patienten als auch Pharmaunternehmen unterstützt. Mangelnde Therapietreue ist ein weit verbreitetes Problem, das selbst hochwirksame Medikamente ineffektiv machen kann. KI-gestützte Smartphone-Apps und digitale Assistenten fungieren inzwischen als persönliche Gesundheitscoaches: Sie erinnern Patienten an die Medikamenteneinnahme, beantworten Fragen über Chatbots und nutzen teilweise sogar Computer Vision, um zu bestätigen, dass eine Dosis tatsächlich eingenommen wurde – beispielsweise durch die Analyse eines Videos, das die Medikamenteneinnahme zeigt. Erste Studien zu solchen KI-Erinnerungssystemen in Europa zeigten verbesserte Therapietreue bei chronischen Erkrankungen wie Bluthochdruck und HIV. Indem diese Werkzeuge sicherstellen, dass Patienten ihre Therapien korrekt und regelmäßig anwenden, tragen sie dazu bei, den Nutzen der Medikamente zu maximieren, was wiederum den Wert der Behandlung bestätigt. Darüber hinaus kann KI-gestützte Überwachung in klinischen Studien die Datenqualität sichern – etwa indem erkannt wird, ob Teilnehmer das Behandlungsschema nicht korrekt einhalten – und «virtuelle Studien» ermöglichen, bei denen Patienten dank zuverlässiger Fernüberwachung seltener Kliniken aufsuchen müssen. All diese Verbesserungen führen dazu, dass Patienten eine reibungslosere Behandlungserfahrung haben – mit weniger Komplikationen, mehr Unterstützung und besseren Ergebnissen –, während Pharmaunternehmen robustere Daten darüber erhalten, wie ihre Medikamente unter realen Bedingungen wirken.
#9 Globale Zusammenarbeit und Initiativen zur Nutzung von KI
Die Revolution an der Schnittstelle von KI, Arzneimittelentwicklung und Patientenversorgung ist ein globales Phänomen, das durch Kooperationen über Länder- und Branchengrenzen hinweg geprägt ist. Tatsächlich entstehen die symbiotischen Effekte häufig aus Partnerschaften: Pharmaunternehmen bringen umfassende Expertise zu Krankheiten und klinischer Forschung ein, Biotech-Start-ups liefern modernste KI-Technologien, und akademische Einrichtungen oder öffentliche Institutionen stellen hochwertige Daten und Validierungsmöglichkeiten bereit. In den vergangenen Jahren hat sich ein klares Muster herausgebildet: Unternehmen und Forschungszentren aus Europa, Nordamerika, Asien und anderen Regionen bündeln ihre Stärken, um das Potenzial von KI im Gesundheitswesen auszuschöpfen. Japan, einer der weltweit größten Pharmamärkte, hat staatlich unterstützte KI-Initiativen gestartet, um die heimische Gesundheitsinnovation zu fördern. Mit Unterstützung der japanischen Regierung und Technologieanbietern wie NVIDIA entwickeln japanische Pharmaunternehmen und Krankenhäuser KI-«Fabriken» für Arzneimittelentwicklung und Patientenversorgung – etwa durch den Einsatz leistungsstarker lokaler Supercomputer zur Entwicklung neuartiger Moleküle oder zur Analyse genomischer Daten der japanischen Bevölkerung für personalisierte Medizin. Diese Bemühungen verdeutlichen ein nationales Engagement für KI in der Pharmaindustrie, das lokale Gesundheitsbedürfnisse – wie die Versorgung einer alternden Bevölkerung – adressiert und gleichzeitig zum globalen Fortschritt beiträgt, etwa durch Japans Beteiligung an internationalen Projekten zur KI-gestützten Krebsforschung und Pandemiebekämpfung.
Auch Südkorea hat stark in KI für die Biotechnologie investiert. Start-ups wie Standigm (bereits zuvor erwähnt) expandieren international und arbeiten mit westlichen Institutionen zusammen, um Fachwissen zu bündeln. Eine aktuelle Kooperation zwischen Standigm und Nashville Biosciences in den USA konzentriert sich auf die Entdeckung neuer Arzneimittelzielstrukturen, indem südkoreanische KI-Algorithmen mit umfangreichen amerikanischen klinischen Datensätzen kombiniert werden. Solche grenzüberschreitenden Partnerschaften verdeutlichen, dass keine einzelne Region ein Monopol auf Innovation besitzt – das Feld entwickelt sich durch geteiltes Wissen weiter. In Europa finanzieren Initiativen wie die Programme von «Horizon Europe» multinationale Konsortien, die KI in Bereichen von der Alzheimer-Arzneimittelentwicklung bis zur Verbesserung der Patientenbeteiligung an klinischer Forschung in den Mitgliedstaaten einsetzen. Gleichzeitig stellen nordamerikanische Technologiekonzerne wie Google, Microsoft und Amazon ihre KI-Plattformen Pharmaunternehmen weltweit zur Verfügung: So helfen beispielsweise das KI-Innovationslabor von Novartis mit Microsoft oder die Kooperation von Pfizer mit AWS im Bereich maschinelles Lernen dabei, KI-Werkzeuge an Forschungsstandorten weltweit zugänglich zu machen. Das Ergebnis all dieser Kooperationen ist ein dynamisches Ökosystem, in dem Erfolge aus einem Teil der Welt – sei es ein neuer KI-designter Wirkstoffkandidat oder eine innovative KI zur Patientenüberwachung – schnell geteilt, validiert und andernorts übernommen werden können. Dieser globale Netzwerkeffekt stellt sicher, dass sowohl die Arzneimittelentwicklung als auch die Patientenversorgung von den neuesten Fortschritten profitieren – unabhängig von ihrem Ursprung. Es handelt sich um eine Symbiose nicht nur zwischen KI und Pharmaindustrie, sondern auch zwischen internationalen Akteuren, die den Innovationszyklus zum Wohle aller beschleunigt.
#10 Gewährleistung von Sicherheit und Pharmakovigilanz durch KI
Sobald neue Therapien Patienten erreichen, ist die Überwachung ihrer Sicherheit und ihrer tatsächlichen Wirksamkeit im Alltag von entscheidender Bedeutung. Auch hier spielt KI zunehmend eine wichtige Rolle, indem sie die Pharmakovigilanz – also die Überwachung der Arzneimittelsicherheit nach der Zulassung – stärkt und Patientenfeedback erfasst, um die weitere Entwicklung zu unterstützen. Pharmaunternehmen und Aufsichtsbehörden beginnen, KI einzusetzen, um die enorme Datenmenge auszuwerten, die nach der Markteinführung eines Medikaments entsteht – von Berichten über Nebenwirkungen und elektronischen Gesundheitsakten bis hin zu Social-Media-Beiträgen, in denen Patienten über Nebenwirkungen sprechen. Algorithmen zur Verarbeitung natürlicher Sprache (Natural Language Processing, NLP) können Zehntausende klinische Sicherheitsberichte oder Patientenkommentare analysieren und potenzielle Sicherheitssignale wesentlich schneller identifizieren als herkömmliche manuelle Prüfverfahren. So hat beispielsweise die Europäische Arzneimittel-Agentur (EMA) KI-Werkzeuge untersucht, um unerwartete Muster von Nebenwirkungen in ihrer EudraVigilance-Datenbank zu erkennen, mit dem Ziel, seltene, aber schwerwiegende unerwünschte Reaktionen früher zu identifizieren, als dies allein menschlichen Analysten möglich wäre. Ebenso hat das Sentinel-Programm der US-amerikanischen FDA, das Gesundheitsversicherungs- und elektronische Gesundheitsdaten zur Arzneimittelsicherheit analysiert, Methoden des maschinellen Lernens integriert, um die Genauigkeit der Signalerkennung zu verbessern und echte Sicherheitsprobleme besser von zufälligem Datenrauschen zu unterscheiden.
Die Fähigkeit der KI, Daten zu integrieren, bedeutet zudem, dass sie Zusammenhänge zwischen Arzneimittelexposition und Behandlungsergebnissen im realen Alltag wesentlich präziser analysieren kann. Dies bringt direkte Vorteile für Patienten: Wenn ein KI-System erkennt, dass eine bestimmte demografische Gruppe oder ein spezifisches genomisches Profil anfälliger für eine unerwünschte Reaktion ist, können Gesundheitsdienstleister gewarnt werden, Vorsichtsmaßnahmen zu treffen oder alternative Therapien für diese Patienten zu wählen. Pharmaunternehmen nutzen solche Erkenntnisse, um die Patientenauswahl und das Risikomanagement in Folgestudien oder bei Indikationserweiterungen zu verbessern. Ein anschauliches Beispiel stammt von einem Medikament gegen Autoimmunerkrankungen, bei dem durch KI-gestützte Analysen von Daten nach der Markteinführung ein leicht erhöhtes Risiko für bestimmte Nebenwirkungen in asiatischen Bevölkerungsgruppen festgestellt wurde. Diese Erkenntnis veranlasste den Hersteller dazu, gemeinsam mit Ärzten in Japan und Korea aktualisierte Empfehlungen zur Überwachung und Dosisanpassung zu entwickeln und dadurch die Patientensicherheit zu erhöhen. Darüber hinaus setzen einige Unternehmen KI-gestützte Chatbots als Form digitaler Patientenbetreuung ein: Diese Systeme können rund um die Uhr mit Patienten interagieren, Fragen zu Medikamenten beantworten und Nutzer dazu auffordern, Nebenwirkungen zu melden, die die KI anschließend bewerten und bei Bedarf an medizinische Teams weiterleiten kann. Dies verbessert nicht nur die Patientenerfahrung – durch sofortige Antworten und personalisierte Unterstützung –, sondern liefert den Unternehmen zugleich wertvolle Echtzeitdaten darüber, wie Medikamente angewendet werden und welche Probleme auftreten. Zusammenfassend stärkt KI das Sicherheitsnetz rund um Patienten, indem sie Probleme frühzeitig erkennt und dazu beiträgt sicherzustellen, dass der Nutzen neuer Medikamente weiterhin die Risiken überwiegt. Sie verkörpert damit die verantwortungsvolle Seite der Innovation, bei der fortschrittliche Technologien genutzt werden, um Vertrauen und Sicherheit bei den Medikamenten zu gewährleisten, auf die Patienten angewiesen sind.
#11 Wachstum des globalen KI-Marktes in Pharma und Biotechnologie (2024–2034)
Die Einführung künstlicher Intelligenz (KI) in der Pharma- und Biotechnologiebranche beschleunigt sich rasant und führt zu einem stark wachsenden globalen Markt. Marktanalysen prognostizieren für den Zeitraum von 2024 bis 2034 ein exponentielles Wachstum von KI-Lösungen sowohl im Pharma- als auch im Biotechnologiesektor, begleitet von hohen durchschnittlichen jährlichen Wachstumsraten (Compound Annual Growth Rate, CAGR).
Marktgröße und CAGR:
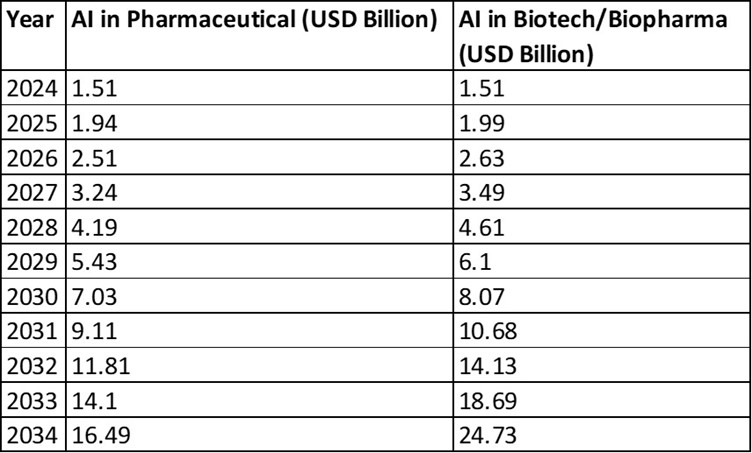
Der globale Markt für KI in der Pharmaindustrie wird voraussichtlich von 1,51 Milliarden US-Dollar im Jahr 2024 auf etwa 16,49 Milliarden US-Dollar bis 2034 anwachsen, was einer CAGR von 27 % im Zeitraum von 2025 bis 2034 entspricht. Gleichzeitig sollen KI-Anwendungen im Biotechnologie- und Biopharma-Sektor von rund 1,51 Milliarden US-Dollar im Jahr 2024 auf 24,73 Milliarden US-Dollar bis 2034 steigen, mit einer noch höheren CAGR von etwa 32,3 % über das Jahrzehnt hinweg. Dieses biopharmazeutische Segment umfasst KI in der Arzneimittelentdeckung, bei Biologika sowie in verwandter biotechnologischer Forschung. Zum Vergleich gehen einige Schätzungen davon aus, dass der KI-Markt in der Biotechnologie im Jahr 2025 bei 2,50 Milliarden US-Dollar liegen und bis 2032 auf etwa 8,56 Milliarden US-Dollar anwachsen wird, was einer CAGR von rund 19 % entspricht und die starken Wachstumsaussichten in der gesamten Branche zusätzlich unterstreicht.
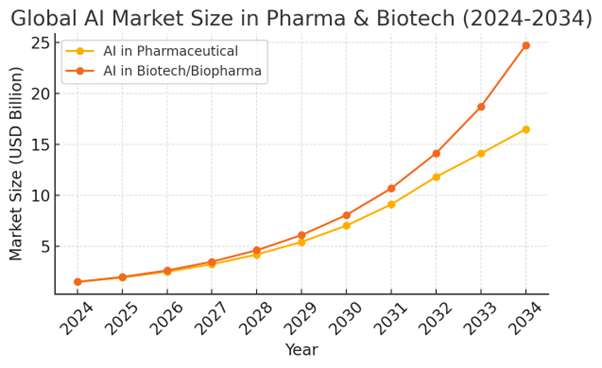
Die nachstehende Tabelle bietet eine jährliche Übersicht über die globale Marktgröße von KI in der Pharma- und Biotechnologiebranche und veranschaulicht den steilen Wachstumstrend:
#12 Reale Auswirkungen von KI auf die Patientenerfahrung weltweit
Künstliche Intelligenz verändert nicht nur Forschung und Entwicklung, sondern gestaltet auch die Art und Weise neu, wie Patienten weltweit medizinische Versorgung erleben. Von Krankenhausstationen bis hin zur häuslichen Überwachung ermöglichen KI-gestützte Plattformen eine intelligentere, schnellere und stärker personalisierte Gesundheitsversorgung. Diese Lösungen reduzieren Komplikationen, verbessern die Therapietreue und unterstützen eine höhere Lebensqualität bei zahlreichen Erkrankungen.
In einem nationalen Gesundheitssystem verhindert eine KI-gesteuerte Lösung für die häusliche Versorgung Notfall-Krankenhauseinweisungen älterer Patienten, indem sie eine klinische Verschlechterung präzise vorhersagt. Behandlungsteams werden frühzeitig informiert und können rechtzeitig eingreifen, um Krisen und Krankenhausaufenthalte zu vermeiden. In der Praxis bedeutet dies, dass Patienten länger, sicherer und selbstbestimmter in ihren eigenen vier Wänden bleiben können – während gleichzeitig die Belastung der Krankenhäuser reduziert wird. Auch andernorts haben Plattformen zur Fernüberwachung von Patienten beeindruckende Ergebnisse erzielt. In einem europäischen Land gingen Krankenhauseinweisungen aufgrund von Herzinsuffizienz dank KI-gestützter virtueller Versorgungsstationen um mehr als 80 Prozent zurück. Auch Patienten mit chronischen Erkrankungen wie COPD oder Risikoschwangerschaften profitieren davon: Sie benötigen weniger Krankenhausbesuche und erhalten rechtzeitig Unterstützung auf Grundlage prädiktiver Warnmeldungen aus tragbaren Sensoren und häuslichen Überwachungssystemen.
In Nordamerika definiert KI-gestützte digitale Therapie die Rehabilitation von Patienten mit chronischen muskuloskelettalen Schmerzen neu. Diese virtuellen Programme begleiten Patienten durch evidenzbasierte Rehabilitationsmaßnahmen, verfolgen ihren Fortschritt in Echtzeit und passen die Behandlung anhand ihrer Reaktionen an. Dadurch werden Schmerzwerte um mehr als 60 Prozent reduziert und die Therapietreue nahezu verdoppelt. In vielen Fällen berichten Patienten sogar, dass sie ihre ursprüngliche Absicht, sich operieren zu lassen, aufgrund der erheblichen funktionellen Verbesserungen durch die KI-gestützte Therapie aufgegeben haben.
Was all diese Innovationen verbindet, ist ihre Fähigkeit, eine kontinuierliche und proaktive Versorgung bereitzustellen. Anstatt sich ausschließlich auf geplante Termine oder von Patienten initiierte Kontaktaufnahmen zu verlassen, analysieren KI-Systeme Daten in Echtzeit, um Unterstützung genau zum richtigen Zeitpunkt bereitzustellen. Das Ergebnis ist eine Versorgung, die nicht nur effizienter, sondern auch menschlicher ist – sie erreicht Patienten dort, wo sie sich befinden, mit genau der Unterstützung, die sie benötigen, und genau dann, wenn sie sie benötigen.
Diese realen Ergebnisse zeigen, wie KI den Zugang zur Gesundheitsversorgung, die Personalisierung von Therapien und die Effizienz der Patientenversorgung verbessert – wodurch weltweit die Systemkosten gesenkt und die Gesundheitsstandards erhöht werden.
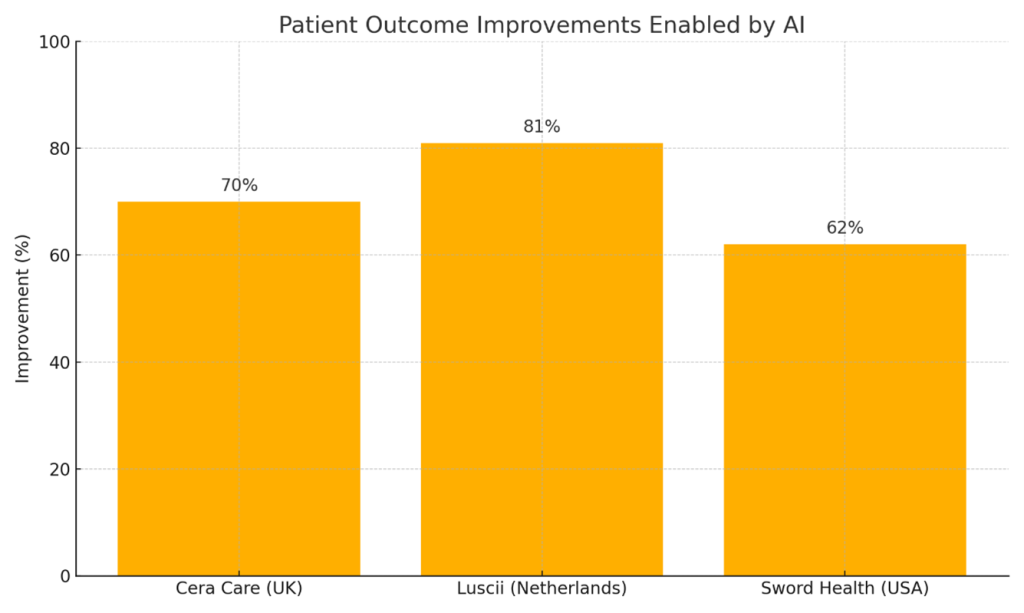
Die folgende Grafik veranschaulicht messbare Verbesserungen der Behandlungsergebnisse von Patienten, die durch KI-gestützte Gesundheitsplattformen ermöglicht wurden, basierend auf realen Anwendungen im Vereinigten Königreich, in den Niederlanden und in den USA.
Fazit
Künstliche Intelligenz hat sich zu einem starken Katalysator in der Pharma- und Biotechnologiebranche entwickelt und schafft eine symbiotische Verbindung zwischen Arzneimittelentwicklung und Patientenerfahrung. Einerseits beschleunigt KI Forschung und Entwicklung – von der Entdeckung neuartiger Wirkstoffkandidaten in Rekordzeit über die Optimierung klinischer Studien bis hin zur Neupositionierung bestehender Medikamente –, was zu einer schnelleren Entwicklung wirksamer Therapien führt. Andererseits verbessern dieselben KI-Fortschritte direkt die Behandlungsergebnisse von Patienten, indem sie personalisierte Therapien ermöglichen, Diagnosen verbessern, die Teilnahme an klinischen Studien vereinfachen und Patienten während der gesamten Behandlung unterstützen. Diese Symbiose zeigt sich weltweit in konkreten Beispielen: KI-designte Medikamente erreichen Jahre früher als erwartet klinische Studien und geben Hoffnung bei Erkrankungen mit wenigen Behandlungsmöglichkeiten; Algorithmen ordnen Patienten den richtigen klinischen Studien zu oder passen Krebstherapien an die individuelle Biologie eines Patienten an; intelligente Systeme sorgen dafür, dass Patienten sicherer versorgt und stärker in ihre Behandlung eingebunden werden. Jeder Erfolg im Labor, der mithilfe von KI erzielt wird, führt letztlich zu einer besseren Erfahrung für Patienten – sei es durch einen schnelleren Zugang zu neuen Medikamenten oder durch ein sichereres und unterstützteres Management chronischer Erkrankungen.
Entscheidend ist, dass diese Fortschritte durch sorgfältige, evidenzbasierte Kooperationen zwischen Technologie- und Medizinexperten erzielt werden, die sich auf reale Daten und strenge Validierungsprozesse stützen. Herausforderungen bleiben bestehen – von der Sicherstellung von Datenqualität und Datenschutz bis hin zur Wahrung einer menschlichen Komponente im Gesundheitswesen –, doch der Fortschritt ist von vorsichtigem Optimismus geprägt. KI ist keine Wunderlösung, aber wie diese Analyse zeigt, ist sie ein vielseitiges Werkzeug, das bei verantwortungsvollem Einsatz bedeutende Fortschritte ermöglicht. Die Pharmaindustrie und Gesundheitsdienstleister lernen nicht nur, mit KI zu koexistieren, sondern aktiv mit ihr zusammenzuarbeiten und Rückkopplungsschleifen zu schaffen, von denen alle Beteiligten profitieren. In dieser symbiotischen Beziehung sind Patienten keine passiven Empfänger von Innovationen; ihre Daten, Bedürfnisse und Erfahrungen prägen die nächste Generation KI-gestützter Lösungen und machen diese stärker patientenzentriert. Die Entwicklung ist eindeutig: Mit der weiteren Reifung der KI wird sich ihr integrierter Einfluss auf die Entwicklung besserer Medikamente und die Bereitstellung einer besseren Patientenversorgung weiter vertiefen. Das Ziel – bessere gesundheitliche Ergebnisse, schneller und individueller bereitgestellt – rückt zunehmend in den Fokus, getragen von einer Partnerschaft zwischen Mensch und KI, die die Komplexität sowohl der Biologie als auch der menschlichen Natur respektiert. Der Weg ist noch lange nicht abgeschlossen, doch jeder Fortschritt bekräftigt das Versprechen, dass KI bei verantwortungsvollem Einsatz weltweit dazu beitragen kann, Heilung zu fördern und Menschen zu stärken.
Ricardo Saltz Gulko
Ricardo Saltz Gulko ist Geschäftsführer von Eglobalis, Mitbegründer und Visionär der European Customer Experience Organization. Er ist ein globaler Stratege, Vordenker und Praktiker im Bereich Kundenerfahrung, der für Samsung und seine Kunden wahrnehmbare Design-Analysen mit Schwerpunkt auf Kundenakzeptanz, -erfahrung und -wachstum erstellt.







